“متغیرات بار مخالف یکدیگر را جذب میکنند؛ بارهای مشابه از هم دور میشوند” اصل اساسی فیزیک پایه است. اما یک مطالعه جدید از دانشگاه آکسفورد که امروز در مجله Nature Nanotechnology منتشر شده است، نشان داده است که ذراتی با بارهای مشابه در محلول، در واقع میتوانند به یکدیگر جذب شوند حتی در فواصل طولانی. همچنین، تیم متوجه شد که این اثر بستگی به بار مثبت و منفی ذرات دارد و به حلال نیز وابسته است.
علاوه بر تغییر باورهای مدتها، این نتایج پیامدهای فوری برای یک دسته از فرآیندها دارد که شامل تعاملات ذرات و مولکولی در طول مقیاسهای مختلف طولی مانند خودترکیبی، بلورسازی و جدایش فازی میشوند.
تیم تحقیقاتی، که در دانشکده شیمی دانشگاه آکسفورد مستقر است، مشاهده کرد که ذرات با بار منفی در فواصل بزرگ یکدیگر را جذب میکنند در حالی که ذرات با بار مثبت دور هم دور میشوند، در حالی که برای حلالهایی مانند الکلها معکوس این اثر مشاهده شد.
این یافتهها شگفتانگیز هستند زیرا به نظر میرسد با اصل مرکزی الکترومغناطیسی که نیروی بین بارهای همان علامت در هر فاصلهای دورنده است، در تضاد باشند.
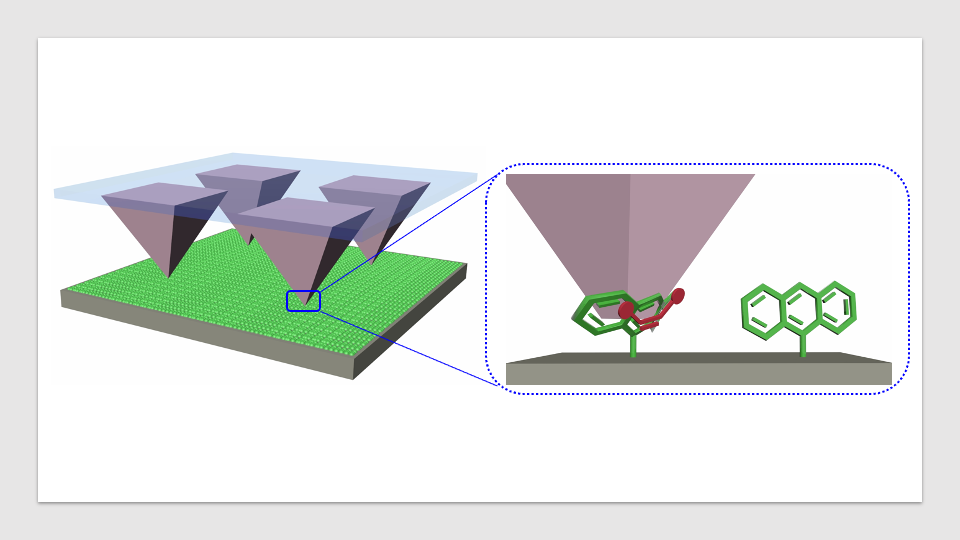
حالا، با استفاده از میکروسکوپ بازتابی روشن، تیم ذرات کوارتزی با بار منفی را در آب معلق کرده و مشاهده کرد که ذرات به یکدیگر جذب میشوند و خوشههای ششضلعی تشکیل میدهند. با این حال، ذرات کوارتزی با بار مثبت خوشهها در آب تشکیل ندادند.
با استفاده از یک نظریه تعاملات ذره به ذره که ساختار حلال را در رابطه در نظر میگیرد، تیم اثبات کرد که برای ذرات با بار منفی در آب یک نیروی جذب وجود دارد که نیروی دورنده الکترواستاتیک را در فواصل بزرگ غالب میکند، به خوشهها منجر میشود. برای ذرات با بار مثبت در آب، این تعامل به دلیل حلال همیشه دورنده است و هیچ خوشهای تشکیل نمیشود.
این اثر به pH وابسته است: تیم توانست تشکیل (یا عدم تشکیل) خوشهها برای ذرات با بار منفی را با تغییر pH کنترل کند. بدون توجه به pH، ذرات با بار مثبت خوشهها را تشکیل ندادند.
بطور طبیعی، تیم متعجب شد که آیا این اثر روی ذرات با بار میتواند تغییر کند، به طوری که ذرات با بار مثبت خوشهها را تشکیل دهند و منفیها نکنند. با تغییر حلال به الکلها مانند اتانول که رفتار رابطه با آب متفاوتی دارد، دقیقاً آنچه را که مشاهده کردهاند را مشاهده کردند: ذرات کوارتزی با بار مثبت خوشههای ششضلعی را تشکیل میدهند، در حالی که کوارتزهای با بار منفی نمیتوانند خوشه تشکیل دهند.
به عقیده محققین، این مطالعه به یک تنظیم مجدد اساسی در درک امور اشاره میکند که بر روی نحوه تفکر در مورد فرآیندهای مختلفی مانند
پایداری محصولات دارویی و شیمیایی دقیق یا اختلال آسیبزا مرتبط با تجمع مولکولی در بیماریهای انسانی تاثیر میگذارد. یافتههای جدید همچنین شواهدی برای توانایی بررسی ویژگیهای پتانسیل الکتریکی رابطهای به علت حلال ارائه میدهند، مانند علامت و مقدار آن که قبلاً غیرقابل اندازهگیری فرض میشد.
استاد مادهاوی کریشنان (دانشکده شیمی، دانشگاه آکسفورد) که این مطالعه را رهبری کرد، میگوید: “من واقعاً از دو دانشجوی کارشناسی ارشدم بسیار مفتخرم، همچنین از دانشجویان کارشناسی که همه با هم برای پیشبرد این کشف اصولی کار کردهاند.”
سیدا وانگ (دانشکده شیمی، دانشگاه آکسفورد)، نویسنده اول مقاله، میگوید: “هنوز هم جذاب است که ببینم این ذرات چگونه جذب یکدیگر میشوند، حتی پس از هزاران بار مشاهده.”
Materials provided by University of Oxford. Note: Content may be edited for style and length.